
ブドウ糖、ソルビトール、クエン酸を原料とする合成多糖である。水に溶けやすい物理化学的特性を有しているが、耐酸性が強く、腸管粘膜の糖類消化酵素によって加水分解を受け難い。
本製品「ファイブミニ」の関与成分であるポリデキストロースの食物繊維としての生理作用が検討されてきた。ラットを対象とする試験において、食物の消化管通過時間の短縮作用及び糞便重量の増加作用が報告されている1)。本製品は、ポリデキストロースの整腸作用、安全性、物理化学的特性に着目し、ポリデキストロースを関与成分とする飲料として開発された。プラセボ対照ヒト試験において、7日間ポリデキストロース 7 gを摂取すると、プラセボ摂取に比べて、糞便の湿重量および水分含量が有意に大きく、糞便硬度が有意に低かった2)。また、試験開始時の排便回数が6回/週以下の被験者では、ポリデキストロース摂取でプラセボ摂取に比べて有意に排便回数が増大した2)。本ヒト試験結果から、表示しようとする保健の用途に必要な関与成分ポリデキストロース量として 7 gが定められた。
【関与成分の構造式】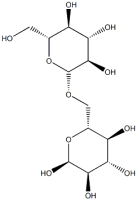 |
(1) Oku et al. J Clin Biochem Nutr 11, 31-40: 1991 (2) 清水精一ら、日本食物繊維研究会誌 1, 25-34: 1997
本品を5分間超音波処理により炭酸を抜く。この液 2 mL を正確に取り、水で50 mL にする。イオン交換樹脂 (アンバーライトIRA-67) 約 3 mL をガラスカラム管に充填し、水10 mL で洗浄した後、調製した試料 4 mL をカラムに通過させる。溶出液を最初から採取し、水を流して溶出液を正確に20 mLとする。この液を0.45μm のメンブランフィルターでろ過し試料溶液とする。
別に定量用ポリデキストロース約3.5 g を秤量し、水で正確に100 mL とする。この溶液 2 mL を正確にとり、水で正確に100 mL とし、標準溶液とする。また、別にテイストオリゴ約 3 g を秤量し、水で正確に100 mL とする。この溶液 1 mL を正確にとり、水で正確に100 mL とし、テイストオリゴ溶液とする。試料溶液、標準溶液及びテイストオリゴ溶液100μLにつき、次の操作条件で液体クロマトグラフ法により試験を行う。それぞれの液のポリデキストロース付近の主ピーク (垂直分割) 面積At、As及びAoを求める。
HPLC 条件
カラム :ULTORON PS-80N 8 mm×30 cm
移動相 :水
検出器 :示差屈折計RI
流量 :1.0 mL/min
カラム温度 :60℃
注入量 :100μL
ポリデキストロース含量 (%)
= Ws × {At- (Ao×2.844/Wo×8/10) / As} × 5/14 × 100
Ws:乾燥物に換算した定量用ポリデキストロースの採取量 (g)
Wo:テイストオリゴの採取量 (g)
定量用ポリデキストロース:カールフィッシャー滴定法で水分を測定する (水分4%以下) 。本品を定量する時、ポリデキスロトースのポリマーとして90%以上を含む。
研究1: 18歳から65歳までの男女38名に、30-60 g/日を12週間摂取させる試験において、随伴症状、血液及び尿症状、血圧、安静時心拍数などに特記すべき異常は認められなかった。 研究2: 2歳から16歳までの男女57名に、0.5-1 g/kgを4週間摂取させる試験において、特記すべき異常は認められなかった。
(1)ファイザー社、中央研究所 Effect of long-term ingestion (12 weeks) at dose levels from 30-60g/day. (2) ファイザー社、中央研究所 Effect in children and adolescents, dose levels of 0.5 to 1.0 g/kg, four weeks (以上、米国FDA提出資料)
研究1: 亜急性毒性試験 (ラット 0 g、1 g、2 g、10 g/kg/日、ビーグル犬 0 g、23 g/kg/日、サル 0 g、1 g、2 g、10 g/kg/日:3ヵ月投与) において、体重増加抑制、軟便、下痢が認められる投与量群は存在したが、毒性の発現は認められなかった。 研究2: マウスに0、5又は10%混餌食を18ヵ月間投与する慢性毒性試験において、ポリデキストロースに起因すると考えられる一般性状、血液検査、行動の異常は観察されなかった。 研究3: ラットの3世代生殖機能試験及び、3世代発癌試験においてもポリデキストロースに起因する毒性、異常は認められなかった。
(1) ファイザー社、中央研究所 ポリデキストロース亜急性毒性試験 (2) ファイザー社、中央研究所 ポリデキストロース亜急性毒性試験 (マウス18ヵ月) (3) ファイザー社、中央研究所 ポリデキストロース亜急性毒性試験 (ラット三世代生殖機能試験) (4) ファイザー社、中央研究所 ポリデキストロース亜急性毒性試験 (ラット三世代発癌性試験) (以上、米国FDA提出資料)
研究1: ポリデキストロースの摂取量の増加に伴い、便が軟らかくなり、ポリデキストロース7及び10 g/日摂取時の便の硬度は無摂取時のそれに比べ有意 (p<0.05) に低い値を示した (1) 。 研究2: ポリデキストロース摂取に伴い、糞便重量は約30%増加し、糞便pHは低下した。また、糞便イソ酪酸、酪酸、イソ吉草酸、吉草酸は著しく低下した。さらに、糞便p-クレゾール、β-グルクロニダーゼ活性は低下した (2) 。 研究3: a)ポリデキストロース含有飲料を用いた盲検試験により、総糞便湿重量、糞便水分含量および糞便硬度が有意に増加した。 b)ポリデキストロース含有飲料を用いた盲検交差試験により、1週間当たり1回以下の女性の排便回数が有意に増加した。
(1) 中川靖枝他:日本栄養・食糧学会誌 43, 95-101: 1990 (2) 遠藤希三子他:腸内フローラと生体ホメオスタシス 31-51: 1988 (3) 清水精一他:日本食物繊維研究会誌 1, 25-34: 1997
研究1: ラットの試験において、ポリデキストロースによる食物の消化管通過時間の短縮作用及び糞便重量の増加作用が報告されている。
Oku et al. J Clin Biochem Nutr 11, 31-40: 1991
